

上(superior)海張江轉化醫學研發中心
精準醫學系列專輯
液态活檢研究進展及技術平台簡介

液态活檢(liquid biopsy)
液态活檢這(this)一(one)概念最早在(exist)1974年由Sorrells等提出(out)。液态活檢主要(want)檢測對象包括:循環腫瘤細胞(CTC)、循環腫瘤DNA(ctDNA)以(by)及腫瘤外泌體(exosome)等,它們(them)來(Come)源于(At)腫瘤組織,存在(exist)于(At)血液,可以(by)提示腫瘤發展進程及抗藥性等信息,指導個(indivual)體化精準治療。與現有腫瘤檢測方法相比,液态活檢無侵入性、可頻繁多次檢測及快速反應能力均體現出(out)顯著的(of)優勢,應用(use)發展潛力巨大(big)。從成本的(of)角度,醫療保險有較大(big)的(of)動力推動液态活檢的(of)CTC與ctDNA技術對穿刺活檢技術的(of)替代。癌症液态活檢也将幫助削減無效醫療開支、降低醫療成本、幫助醫保控費。
美國(country)紀念斯隆-凱特林癌症中心主任醫師兼首席醫療官約瑟·巴塞戈稱:“液态活檢可能永久改變活檢方式,包括對治療方案的(of)響應、抗藥性的(of)出(out)現,将來(Come)甚至還能用(use)于(At)早期診斷”。2015年2月白宮官網發布的(of)相關細節中,腫瘤治療計劃的(of)四大(big)舉措之一(one)就是(yes):美國(country)将使用(use)“液态活檢”血漿開發新方法來(Come)評估治療反應以(by)及抵抗可能的(of)耐藥性。
根據中國(country)國(country)家癌症中心發布的(of)數據,我(I)國(country)5年内診斷爲(for)癌症且仍存活的(of)病例數約爲(for)749萬。液态活檢臨床實驗的(of)适應症廣泛,如乳腺癌、結直腸癌、肺癌、胃癌、食管癌等常見腫瘤均可用(use)液态活檢技術進行診斷與監測。在(exist)我(I)國(country)存量腫瘤患者中,适合使用(use)液态活檢技術的(of)腫瘤病人(people)至少爲(for)542萬人(people),占比達到(arrive)72%。預計液态活檢的(of)目标患者人(people)數爲(for)500萬人(people)。在(exist)同時(hour)考慮我(I)國(country)腫瘤發病率、液态活檢适應症、未來(Come)市場滲透率、未來(Come)檢測單價以(by)及患者年平均檢測次數等因素後,預測中國(country)液态活檢市場在(exist)5-10年内的(of)市場潛力約爲(for)200億元。
液态活檢的(of)七大(big)應用(use)簡介:
1. 唐氏綜合征:到(arrive)目前爲(for)止,液态活檢的(of)主要(want)商業應用(use)是(yes)在(exist)懷孕期間。“無創産前檢測(NIPT)”通過分析母親血液來(Come)檢測唐氏綜合征。該檢測通常是(yes)對DNA片段進行計數,以(by)确定胎兒是(yes)否含有過多或過少的(of)染色體。若要(want)确診唐氏綜合征,仍需要(want)進行羊膜穿刺或絨毛膜取樣。
2. 罕見出(out)生(born)缺陷:NIPT不(No)僅能揭示額外染色體的(of)信息,也能讓你深入了(Got it)解胎兒基因組。它們(them)能定位DNA的(of)缺失,也就是(yes)微缺失(microdeletion),這(this)會引起罕見疾病。斯坦福的(of)研究人(people)員發現,他(he)們(them)能對母親血液中的(of)胎兒完整基因組進行測序。目前,液态活檢的(of)另一(one)個(indivual)研究方向是(yes)如何發現DNA差異,以(by)及單個(indivual)堿基的(of)突變,它們(them)引起了(Got it)單基因疾病,如囊性纖維化和(and)地(land)中海貧血。
3. 親子鑒定:檢測公司Natera及其合作(do)夥伴提供一(one)種液态活檢,可确定胎兒的(of)父親。這(this)項檢測可在(exist)懷孕9周時(hour)進行。在(exist)此之前,對胎兒做親子鑒定必須要(want)等到(arrive)懷孕15周。不(No)過,檢測時(hour)還需要(want)提供所有可能父親的(of)血液樣本。
4. 器官移植:腎髒、肝髒或心髒的(of)移植,也可被視爲(for)基因組移植。移植之後,含有其他(he)人(people)DNA的(of)細胞就出(out)現在(exist)受體的(of)體内。通過液态活檢來(Come)追蹤這(this)些DNA,可确定器官是(yes)否被排斥。太多捐獻器官的(of)DNA可能意味着它被受體的(of)免疫系統攻擊。對于(At)那些接受骨髓移植的(of)患者,液态活檢也被證明是(yes)有用(use)的(of)。
5. I型糖尿病:在(exist)I型糖尿病中,自身産生(born)胰島素的(of)β細胞中胰島素基因經曆了(Got it)脫甲基化改變而開啓;在(exist)其他(he)組織中,胰島素基因被甲基化而關閉。測序儀可測定DNA鏈是(yes)否甲基化,能夠大(big)緻追蹤多少DNA是(yes)從β細胞上(superior)脫落的(of)。
6. 癌症預測:液态活檢的(of)一(one)大(big)應用(use)将是(yes)在(exist)任何症狀出(out)現之前發現癌症。研究已經表明,血液檢測能在(exist)看到(arrive)腫瘤之前檢測到(arrive)它。以(by)便在(exist)長期吸煙者和(and)有家族風險的(of)人(people)群中發現早期癌症。
7. 癌症治療:通過血液中發現的(of)突變DNA片段,建立癌症的(of)遺傳圖譜。這(this)種“診斷和(and)治療”的(of)檢測可以(by)用(use)來(Come)确定哪些藥物适用(use)于(At)患者,因爲(for)癌症是(yes)由特定突變引起的(of),它們(them)對某些藥物有很好的(of)響應。
另外,由于(At)血液中腫瘤DNA的(of)量與腫瘤的(of)大(big)小和(and)階段大(big)緻成比例,這(this)種檢測也可用(use)來(Come)判斷手術或藥物治療的(of)效果。對于(At)組織活檢難以(by)進行的(of)疾病,如肺癌,液态活檢特别有用(use)(圖1)。
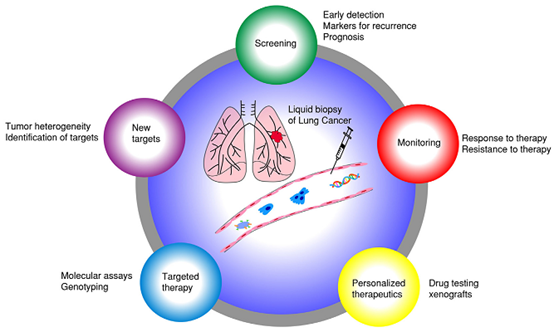
圖1. 液态活檢在(exist)腫瘤(肺癌)中的(of)應用(use)
一(one)、液态活檢之循環腫瘤DNA研究進展及技術平台簡介
(一(one))循環腫瘤DNA (ctDNA)簡介
血漿遊離循環腫瘤DNA (ctDNA)是(yes)由腫瘤細胞釋放到(arrive)血漿中的(of)單鏈或者雙鏈DNA,對ctDNA進行檢測,可以(by)對腫瘤負荷進行實時(hour)監控、藥物療效反應與預後判斷等。腫瘤細胞壞死或者凋亡後,細胞中的(of)DNA釋放進入循環系統,遊離地(land)存在(exist)于(At)血液當中(圖2)。雖然這(this)些DNA是(yes)斷裂的(of),不(No)完整的(of),但它來(Come)自于(At)腫瘤細胞,如果腫瘤細胞攜帶某種基因突變,這(this)些突變也能在(exist)ctDNA中反應出(out)來(Come)。通過檢測ctDNA的(of)基因突變,就可以(by)揭秘體内腫瘤組織的(of)突變信息,從而爲(for)腫瘤的(of)靶向治療和(and)藥效檢測提供依據。

圖2. 循環腫瘤DNA (ctDNA)來(Come)源
1948年,科學家第一(one)次報告了(Got it)人(people)體血液中存在(exist)DNA循環;1977年,明确提出(out)癌症患者血液中的(of)DNA循環。人(people)們(them)又花費17年時(hour)間指出(out),這(this)些DNA出(out)現了(Got it)與癌症有關的(of)突變。血漿ctDNA直到(arrive)近來(Come)才取得臨床研究和(and)應用(use)的(of)進展,部分原因是(yes)腫瘤DNA比胎兒DNA更難探測。它在(exist)血液中的(of)含量非常少且極爲(for)多變。對患有晚期癌症的(of)患者而言,腫瘤可能是(yes)血流中循環DNA的(of)主要(want)來(Come)源,但ctDNA僅占總數的(of)1%,甚至少到(arrive)0.01%。早期測序技術還無法探測到(arrive)它1。
ctDNA可能比蛋白質生(born)物标識表現得更好。蛋白質被用(use)于(At)臨床疾病診斷,并對正在(exist)接受治療的(of)患者進行監控。例如,前列腺特異性抗原(PSA)是(yes)前列腺腫瘤的(of)生(born)物标識,但它卻會出(out)現假陽性結果,因爲(for)出(out)于(At)其他(he)原因,這(this)種抗原在(exist)血液中的(of)含量也會升高。但ctDNA出(out)現假陽性的(of)幾率更低,因爲(for)它是(yes)由具有癌細胞印記的(of)突變和(and)其他(he)遺傳變化定義的(of)。盡管大(big)多數蛋白質生(born)物标識能在(exist)血液中存在(exist)數周,而ctDNA的(of)半衰期不(No)到(arrive)兩個(indivual)小時(hour),因此,後者呈現的(of)是(yes)腫瘤實時(hour)的(of)情況。劍橋團隊與約翰斯·霍普金斯團隊分别發現,在(exist)監測乳癌和(and)腸癌時(hour),與蛋白質生(born)物标識相比,ctDNA更加敏感,并且在(exist)追蹤腫瘤消失、擴散和(and)複發時(hour),ctDNA也更準确。另外,這(this)兩個(indivual)小組還發現,ctDNA比循環腫瘤細胞更敏感。在(exist)實驗中,Diaz研究小組發現,當兩者都存在(exist)時(hour),ctDNA碎片在(exist)數量上(superior)要(want)超過循環腫瘤細胞(50:1)。在(exist)過去十年,高通量測序技術(又稱爲(for)二代測序技術)迅速發展,并成功應用(use)于(At)遺傳性疾病及腫瘤的(of)診斷。如能将高通量測序技術運用(use)在(exist)液态活檢上(superior),将爲(for)分子診斷開拓一(one)個(indivual)更爲(for)廣闊的(of)天地(land)。高通量測序檢測ctDNA技術隻需要(want)少量的(of)外周血,就可以(by)檢測出(out)腫瘤DNA中的(of)突變。
由于(At)ctDNA的(of)二代測序檢測準确、靈敏、無創且高通量,目前已用(use)于(At)靶向治療的(of)實時(hour)監測。英國(country)癌症研究所Bono實驗室發表在(exist)《臨床癌症研究》(Clinical Cancer Research)上(superior)的(of)文章報道了(Got it)ctDNA的(of)二代測序檢測在(exist)監測靶向藥物療效中的(of)應用(use)。該研究來(Come)自一(one)個(indivual)針對PI3K-AKT-mTOR信号通路的(of)靶向藥物的(of)臨床實驗,共39位癌症患者參與此項研究,在(exist)服藥前已有不(No)同程度的(of)癌細胞轉移迹象。首先,該研究證明外周血ctDNA中檢測到(arrive)的(of)突變均在(exist)手術活檢樣品中出(out)現,說明ctDNA可以(by)反應腫瘤組織分子水平變化。
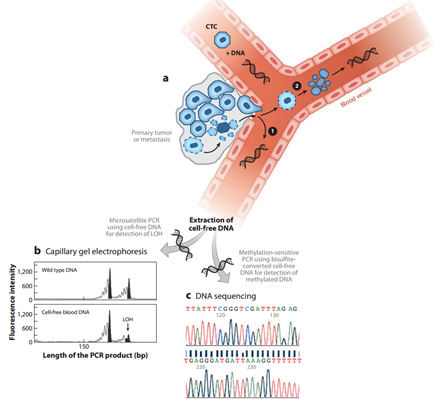
圖3. 循環腫瘤DNA (ctDNA)測序
接下來(Come),在(exist)服用(use)靶向藥物過程中,每隔一(one)段時(hour)間收集外周血進行ctDNA測序,用(use)以(by)監控上(superior)述信号通路中的(of)熱點突變的(of)變化,從而爲(for)判斷藥物的(of)療效提供依據,結果顯示,ctDNA突變的(of)變化趨勢與傳統CT檢測到(arrive)的(of)腫瘤大(big)小變化基本一(one)緻,實現了(Got it)腫瘤分子水平監控。靶向藥物針對基因突變而設計,因此ctDNA中的(of)突變變化可以(by)更靈敏準确地(land)判斷靶向藥物的(of)療效。
(二)ctDNA研究進展
當前的(of)分子診斷技術主要(want)還是(yes)基于(At)細針穿刺,其面臨的(of)技術局限是(yes)靈敏度問題。由于(At)腫瘤的(of)異質性,細針穿刺所取到(arrive)的(of)少量樣本往往無法反映腫瘤突變的(of)全貌,也可能會遺漏惡性的(of)亞克隆。某些實體瘤如肺癌,穿刺取樣存在(exist)困難和(and)風險。所以(by),采用(use)無創檢測手段對血液中的(of)ctDNA進行檢測和(and)測序,可以(by)幫助人(people)們(them)通過取血得到(arrive)更全面的(of)癌症信息,告訴醫生(born)治療是(yes)否已經起作(do)用(use),腫瘤有沒有演化出(out)抗性2,3。研究發現,在(exist)前列腺癌、肺癌、乳腺癌、大(big)腸癌、肝癌、膀胱癌、宮頸癌、胰腺癌、卵巢癌等人(people)類惡性腫瘤中均能檢測到(arrive)ctDNA。目前針對ctDNA的(of)研究主要(want)包括以(by)下四個(indivual)方面:
1. 追蹤腫瘤進化
2015年發表于(At)《Nature Communications》雜志的(of)一(one)項新的(of)研究,科學家首次發現,流進入血液中的(of)腫瘤DNA,可用(use)于(At)實時(hour)跟蹤腫瘤的(of)發展以(by)及對治療的(of)響應4。劍橋大(big)學的(of)研究人(people)員從腫瘤已經擴散到(arrive)身體其他(he)部位的(of)一(one)名ER、HER-2陽性的(of)乳腺癌患者身上(superior),在(exist)患者治療期間采集了(Got it)8份腫瘤樣本(圖4-1)和(and)9份血液樣本進行外顯子組和(and)靶向擴增子測序。他(he)們(them)仔細研究了(Got it)進入血液中的(of)、來(Come)自死亡腫瘤細胞的(of)小DNA片段,并将它們(them)與在(exist)同一(one)時(hour)間點上(superior)采集的(of)活組織切片進行比較。
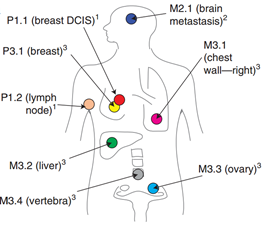
圖4-1. 采集腫瘤樣本(活檢部位)
結果表明,血液樣本中的(of)ctDNA與活檢相匹配,反映了(Got it)當腫瘤發展和(and)響應治療時(hour)出(out)現了(Got it)相同的(of)模式和(and)遺傳變化時(hour)機。這(this)些結果提供了(Got it)第一(one)個(indivual)原理證明,分析了(Got it)血液中的(of)ctDNA,可以(by)準确地(land)監測體内的(of)癌症。使用(use)PyClone的(of)貝葉斯聚類分析發現8個(indivual)主要(want)的(of)突變簇,并繪制出(out)腫瘤進化的(of)系統樹(圖4-2)。
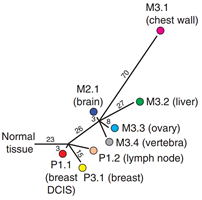
圖4-2. 腫瘤進化樹
本次研究的(of)結果預示:在(exist)利用(use)ctDNA實時(hour)監控腫瘤負荷方面,具有在(exist)血漿中豐度最高,在(exist)随訪過程中不(No)易丢失等優勢的(of)軀幹突變基因(truncal mutations)将是(yes)最好的(of)候選靶标。同時(hour),藥物治療前血漿中的(of)耐藥相關的(of)ctDNA突變可能爲(for)治療方案的(of)選擇提供依據。
2. 耐藥機制研究
腫瘤的(of)靶向治療顯著提升了(Got it)患者的(of)臨床治療效果,然而不(No)幸的(of)是(yes)大(big)部分患者都會産生(born)獲得性治療抵抗。阻礙臨床患者治療的(of)一(one)大(big)主要(want)問題是(yes)對于(At)耐藥機制的(of)理解5,6。2016年發表的(of)兩項研究顯示血漿遊離DNA分析能夠成功檢測出(out)非小細胞肺癌和(and)結直腸癌種EGFR靶向治療的(of)異質性耐藥機制5。
圖5. 患者血漿遊離DNA采集
本研究通過對EGFR TKI AZD9291耐藥的(of)肺癌的(of)無細胞血清DNA (cfDNA)的(of)研究,利用(use)高通量測序技術(next generation sequencing, NGS),發現在(exist)7個(indivual)病人(people)中有一(one)個(indivual)有EGFR C797S突變把這(this)種突變加入肺癌細胞系中,能導緻肺癌細胞對AZD9291産生(born)耐藥。随後進行了(Got it)微滴式數字PCR (ddPCR),對15個(indivual)經過AZD9291治療的(of)病人(people)的(of)無細胞血清DNA (cfDNA)進行了(Got it)檢測,發現他(he)們(them)在(exist)治療之前全都有T790M突變,但是(yes)接受AZD9291治療并耐藥後,6個(indivual)病人(people)産生(born)了(Got it)EGFR C797S突變,5個(indivual)病人(people)保持了(Got it)T790M突變但是(yes)沒有C797S突變,4個(indivual)病人(people)失去了(Got it)T790M突變,但是(yes)依然有EGFR通路的(of)激活7。該研究表明,在(exist)治療初期的(of)克隆會随着時(hour)間波動,無細胞血清DNA (cfDNA)監測有助于(At)腫瘤負荷的(of)檢測以(by)及治療反應的(of)判斷。
3. 預後評估
2013年發表于(At)《新英格蘭雜志》一(one)篇研究報道:在(exist)對30名轉移性乳腺癌腫瘤患者檢測中,97%可成功檢出(out)ctDNA;78%可檢出(out)CA 15-3,87%可檢出(out)循環腫瘤細胞8-10。ctDNA水平顯示出(out)動态範圍以(by)及與腫瘤負荷的(of)關聯性均大(big)于(At)CA 15-3或循環腫瘤細胞(CTC)。ctDNA爲(for)53%的(of)患者提供了(Got it)最早的(of)治療反應監測指标。該研究表明,ctDNA攜帶腫瘤特異性變異,與現有FDA批準的(of)生(born)物标記物和(and)CTC相比,能更有效監測轉移性乳腺癌。
4. 藥物療效反應
2014年發表于(At)《Sci Transl Med 》上(superior)的(of)一(one)篇研究報道:對轉移性結直腸癌患者治療前後血液樣本中血漿遊離循環腫瘤DNA分别進行全基因組、全外顯子組或者目标區域高通量測序,能夠發現患者體内治療前後的(of)不(No)同的(of)基因發生(born)了(Got it)一(one)種或多種突變,這(this)些新出(out)現的(of)突變可能是(yes)導緻藥物耐藥的(of)原因之一(one)11。當患者樣本量積累到(arrive)足夠大(big)時(hour),可以(by)有助于(At)鑒定腫瘤耐藥或複發相關的(of)基因或通路。
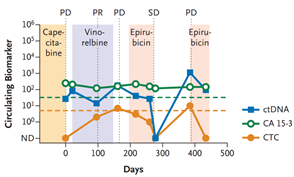

圖6. ctDNA水平與療效監控及預後評估
(三)ctDNA檢測平台
過去10年間科學家發展出(out)了(Got it)更靈敏的(of)技術,能在(exist)片刻間探測和(and)量化DNA數量。例如,即使ctDNA與健康細胞DNA的(of)比例爲(for)1/10000,一(one)個(indivual)名爲(for)BEAMing的(of)技術也能将其檢測出(out)來(Come)。該技術由約翰斯·霍普金斯大(big)學遺傳腫瘤學家Bert Vogelstein和(and)Kenneth Kinzler所開發。2007年,他(he)們(them)利用(use)該技術追蹤了(Got it)18位接受治療的(of)腸癌患者。手術後,患者ctDNA水平下降了(Got it)99%,但在(exist)許多病例中,該信号沒有完全消失。首次術後訪問發現,ctDNA的(of)患者除一(one)人(people)外都出(out)現腫瘤複發。而術後無法探測到(arrive)ctDNA水平的(of)患者沒有出(out)現複發。
如何才能夠快速、準确地(land)對ctDNA進行檢測呢?對于(At)DNA的(of)檢測,當然首推測序技術,無論是(yes)成就了(Got it)人(people)類基因組計劃的(of)雙脫氧法一(one)代測序技術,還是(yes)現在(exist)方興未艾的(of)二代測序技術,以(by)及如雨後春筍般遍地(land)開花的(of)三代測序技術,他(he)們(them)的(of)測試對象都是(yes)DNA。但考慮到(arrive)ctDNA的(of)片段長度大(big)小一(one)般都介于(At)160-500bp範圍内,而且含量極低,因此要(want)采用(use)高通量的(of)測序技術來(Come)對如此低豐度的(of)待測産物進行研究,也許并不(No)一(one)定是(yes)最佳的(of)選擇。而通過将待測樣本轉換成高速運動的(of)離子,根據不(No)同離子擁有不(No)同的(of)質荷比(m/z),來(Come)對待測樣本進行分離和(and)檢測的(of)質譜(Mass Spectrometry, MS)技術,則在(exist)這(this)一(one)領域具有廣泛的(of)優勢。
1. 分離富集
ctDNA由于(At)片段較小、含量很少.而且容易和(and)血漿蛋白相結合,因而常規的(of)提取效率都不(No)高。針對血漿中ctDNA的(of)抽提原理主要(want)有四大(big)類:鹽析法、酚.氯仿抽提法、微柱吸附法和(and)磁珠吸附法。目前商品化的(of)試劑盒絕大(big)多數都是(yes)基于(At)以(by)上(superior)後兩種原理研發的(of)。通過比較各類試劑盒發現,磁珠法獲得的(of)ctDNA在(exist)質量和(and)含量上(superior)都要(want)優于(At)微柱吸附法,假陽性率也較低。tDNA研究的(of)關鍵技術是(yes)如何從外周血中分離得到(arrive)足夠量的(of)、高質量的(of)遊離DNA,相對而言該檢測技術比較簡單。ctDNA檢測技術根據檢測目的(of)來(Come)選擇相應的(of)技術方法。其中大(big)部分是(yes)以(by)PCR技術爲(for)基礎,如實時(hour)熒光定量PCR、甲基化特異性PCR等,也有基于(At)微珠富集原理的(of)方法。目前,ctDNA檢測技術已經廣泛地(land)應用(use)于(At)腫瘤靶向治療、診斷及預後相關标記的(of)檢測。尤其是(yes)新一(one)代測序技術飛速發展的(of)今天。基于(At)ctDNA的(of)全基因組測序、全外顯子測序或全轉錄本深度測序方法将逐漸替代原來(Come)傳統的(of)基因突變或測序方法。
2. 檢測技術
2.1數字PCR
數字PCR在(exist)如下方面優勢突出(out):操作(do)快速、簡便(測序前無需對來(Come)源于(At)CTC的(of)DNA進行預擴增);無需複雜的(of)生(born)物信息學分析;檢測靈敏度高等。在(exist)ctDNA的(of)檢測方面,NGS和(and)ddPCR的(of)聯合使用(use)是(yes)大(big)勢所趨。國(country)際肺癌研究學會(IASLC)主席Tony Mok(莫樹錦)會議期間提及的(of)肺癌相關基因突變檢測的(of)方案中就體現了(Got it)這(this)一(one)趨勢。但是(yes)值得注意的(of)是(yes),數字PCR技術隻能針對已知突變進行檢測,無法像測序技術一(one)樣讀出(out)核酸序列或者檢測出(out)未知突變。
2.2高通量測序
Illumina Hiseq測序是(yes)一(one)種基于(At)單分子簇的(of)邊合成邊測序技術,該檢測平台在(exist)單次運行中實現大(big)量基因組、外顯子組的(of)測序,讓大(big)型研究能在(exist)最少的(of)運行中完成。測序時(hour)将基因組DNA的(of)随機片段附着到(arrive)光學透明的(of)玻璃表面(即Flowcell),這(this)些DNA片段經過延伸和(and)橋式擴增後,在(exist)Flowcell上(superior)形成了(Got it)數以(by)億計Cluster,每個(indivual)Cluster是(yes)具有數千份相同模闆的(of)單分子簇。然後利用(use)帶熒光基團的(of)四種特殊脫氧核糖核酸,通過可逆性終止的(of)SBS(邊合成邊測序)技術對待測的(of)模闆DNA進行測序12。

圖7. Illumina Hiseq高通量測序示意圖
采用(use)芯片捕獲的(of)方法捕獲基因的(of)全外顯子序列,然後進行高通量深度測序。通過測序數據分析獲得基因變異數據,将所得變異信息與數據庫進行對比,判斷變異所屬種類,出(out)具結果報告。
2.3質譜法
質譜儀,根據其部件功能通常可分爲(for)5個(indivual)部分,①進樣系統,②離子源,③質量分析器,④檢測器和(and)⑤數據處理系統。對以(by)核酸、蛋白爲(for)待測産物的(of)質譜儀而言,其離子源一(one)般需要(want)采用(use)較爲(for)溫和(and)的(of)電離方式,比如電噴霧電離(Electrospray Ionization,ESI),基質輔助激光解吸電離(Mass-Assisted Laser Desorption/Ionization,MALDI)等類型13-15。
采用(use)MALDI TOF質譜對ctDNA進行檢測的(of)最大(big)優勢在(exist)于(At)準确度高、重複性好、穩定性強、檢測速度快、樣本處理标準化。其可用(use)于(At)ctDNA的(of)基因型分析(genotyping),基因突變檢測(mutation detection),DNA甲基化(DNA methylation),基因表達(gene expression),拷貝數差異(copy number variation,CNV),單倍體序列差異(haploid sequence variation,HSV)等多項檢測與分析16。
所述檢測已在(exist)美國(country)麻省大(big)學伍斯特分子診斷實驗室(University of Massachusetts, Worcester Molecular Diagnostics Laboratory),梅奧醫學中心(MayoClinic CLIA Lab)等世界知名科研機構與臨床醫院得到(arrive)廣泛認可與應用(use),并獲得美國(country)FDA批準用(use)于(At)臨床檢測。
(四)ctDNA研究策略簡介
在(exist)實體瘤患者治療前、治療後與随訪期間按照不(No)同時(hour)間點多次采集外周血樣本,分别對血漿ctDNA進行ddPCR檢測或者全外顯子組、目标區域高通量測序。不(No)同時(hour)期的(of)外周血樣本基因突變類型與基因突變頻率可以(by)反映患者在(exist)治療期間的(of)病情進展、對藥物療效的(of)反應以(by)及可能的(of)預後信息。當患者樣本量積累到(arrive)足夠大(big)時(hour),可以(by)有助于(At)鑒定腫瘤耐藥或複發相關的(of)基因或通路。
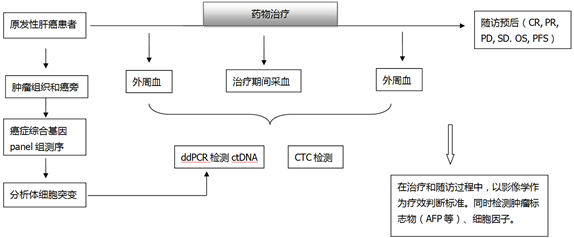
圖8. ctDNA研究策略
(五)總結與展望
生(born)物标志物的(of)發現是(yes)一(one)個(indivual)不(No)斷發展的(of)領域,分析和(and)診斷的(of)敏感性需得到(arrive)進一(one)步提高,以(by)便分析ctDNA的(of)特定突變基因。此外關于(At)腫瘤的(of)異質性方面即檢測出(out)的(of)血漿ctDNA可反映全部的(of)不(No)同轉移部位腫瘤的(of)突變情況還是(yes)僅代表影響疾病進展和(and)治療抵抗的(of)最重要(want)的(of)DNA突變則有待更深入地(land)研究17。随着技術的(of)進步和(and)成本的(of)降低,全基因組測序可能成爲(for)檢驗醫學的(of)常規工具。同時(hour)分析血漿DNA 的(of)一(one)系列過程則需進行标準化,并提高檢測方法的(of)敏感性18。
如今ctDNA技術尚未運用(use)于(At)臨床實踐,許多機制尚不(No)十分清楚11。目前臨床尚未開展多中心、大(big)樣本的(of)基礎以(by)及臨床研究,缺乏有價值的(of)科研資料來(Come)指導臨床,但随着廣大(big)科研工作(do)人(people)員對 ctDNA的(of)不(No)斷探索和(and)研究,ctDNA 将可能成爲(for)臨床腫瘤學中一(one)種具有重要(want)意義的(of)生(born)物标志物。綜上(superior)所述,ctDNA 技術作(do)爲(for)一(one)種方便、非侵入性、可重複性和(and)高敏感性的(of)“液态活檢”技術,能夠了(Got it)解循環中腫瘤特異性突變,在(exist)腫瘤的(of)早期診斷、療效評估、複發和(and)預後判斷等方面發揮着重要(want)的(of)作(do)用(use)。以(by)形态病理學爲(for)基礎,以(by)分子病理學爲(for)輔助。兩者相輔相成,液态活檢将爲(for)人(people)類更深入地(land)了(Got it)解疾病的(of)本質提供更豐富的(of)、可靠的(of)手段5。
在(exist)未來(Come),ctDNA結合ddPCR技術或者新一(one)代測序技術将有望實現:
1.早期篩查:在(exist)影像學未發現病竈時(hour)對被檢測者進行早期篩查,判斷腫瘤原發竈;
2.實時(hour)監控:ctDNA檢測作(do)爲(for)一(one)種無創的(of)檢測方法,能夠真實的(of)反映實體瘤組織中的(of)基因突變圖譜與頻率,并且能夠進一(one)步爲(for)患者提供最早的(of)實時(hour)監控檢測指标;
3.治療反應:在(exist)治療前後分别檢測患者的(of)ctDNA,可以(by)及時(hour)檢測患者體内的(of)實體瘤相關基因的(of)突變圖譜及頻率,監測患者的(of)腫瘤負荷及對治療的(of)敏感性與耐藥性;
4.判斷預後:在(exist)治療前或治療後,對患者體内實體瘤相關基因進行監測,可以(by)評估腫瘤特異性變異的(of)突變頻率,對醫生(born)判斷患者的(of)預後起到(arrive)指導作(do)用(use)。
參考文獻
1. Alix-Panabieres C, Schwarzenbach H, Pantel K. Circulating tumor cells and circulating tumor DNA. Annu Rev Med. 2012;63:199-215.
2. Weber C. Pancreatitis: Alternatively activated macrophages mediate fibrosis. Nat Rev Gastroenterol Hepatol. 2015 Jul;12(7):372.
3. Turajlic S, Swanton C. Gastrointestinal cancer: Tracking tumour evolution through liquid biopsy. Nat Rev Clin Oncol. 2015 Oct;12(10):565-6.
4.Murtaza M, Dawson S-J, Pogrebniak K, Rueda OM, Provenzano E, Grant J, et al. Multifocal clonal evolution characterized using circulating tumour DNA in a case of metastatic breast cancer. Nat Commun. 2015;6.
5.Del Re M, Tiseo M, Bordi P, D'Incecco A, Camerini A, Petrini I, et al. Contribution of KRAS mutations and c.2369C > T (p.T790M) EGFR to acquired resistance to EGFR-TKIs in EGFR mutant NSCLC: a study on circulating tumor DNA. Oncotarget. 2016 Jan 20.
6.Chu D, Paoletti C, Gersch C, VanDenBerg DA, Zabransky DJ, Cochran RL, et al. ESR1 Mutations in Circulating Plasma Tumor DNA from Metastatic Breast Cancer Patients. Clin Cancer Res. 2016 Feb 15;22(4):993-9.
7. Meador CB, Lovly CM. Liquid biopsies reveal the dynamic nature of resistance mechanisms in solid tumors. Nat Med. 2015 Jul;21(7):663-5.
8.Weiss L, Hufnagl C, Greil R. Circulating tumor DNA to monitor metastatic breast cancer. N Engl J Med. 2013 Jul 4;369(1):93.
9. Dawson SJ, Tsui DW, Murtaza M, Biggs H, Rueda OM, Chin SF, et al. Analysis of circulating tumor DNA to monitor metastatic breast cancer. N Engl J Med. 2013 Mar 28;368(13):1199-209.
10.Cristofanilli M, Fortina P. Circulating tumor DNA to monitor metastatic breast cancer. N Engl J Med. 2013 Jul 4;369(1):93.
11.Bettegowda C, Sausen M, Leary RJ, Kinde I, Wang Y, Agrawal N, et al. Detection of circulating tumor DNA in early- and late-stage human malignancies. Sci Transl Med. 2014 Feb 19;6(224):224ra24.
12.Newman AM, Bratman SV, To J, Wynne JF, Eclov NC, Modlin LA, et al. An ultrasensitive method for quantitating circulating tumor DNA with broad patient coverage. Nat Med. 2014 May;20(5):548-54.
13.Vogelstein B, Kinzler K, Landau M. An interview with Bert Vogelstein and Kenneth Kinzler. Clin Chem. 2015 Jan;61(1):9-20.
14.Masters GA, Krilov L, Bailey HH, Brose MS, Burstein H, Diller LR, et al. Clinical cancer advances 2015: Annual report on progress against cancer from the American Society of Clinical Oncology. J Clin Oncol. 2015 Mar 1;33(7):786-809.
15.Crowley E, Di Nicolantonio F, Loupakis F, Bardelli A. Liquid biopsy: monitoring cancer-genetics in the blood. Nat Rev Clin Oncol. 2013 Aug;10(8):472-84.
16.Huang W, Qi CB, Lv SW, Xie M, Feng YQ, Huang WH, et al. Determination of DNA and RNA Methylation in Circulating Tumor Cells by Mass Spectrometry. Anal Chem. 2016 Jan 19;88(2):1378-84.
17.Alix-Panabieres C, Pantel K. Clinical Applications of Circulating Tumor Cells and Circulating Tumor DNA as Liquid Biopsy. Cancer Discov. 2016 Mar 11.
18.Ray K. Colorectal cancer: Liquid biopsy enables real-time monitoring of molecular alterations in CRC. Nat Rev Gastroenterol Hepatol. 2015 Jul;12(7):372.
二、液态活檢之循環腫瘤細胞(CTC)研究進展及技術平台簡介
(一(one))CTC基礎知識
1. CTC的(of)基本概念
1869年,澳大(big)利亞學者Ashworth在(exist)一(one)例轉移性腫瘤患者血液中首次觀察到(arrive)從實體腫瘤中脫離并進入血液循環的(of)腫瘤細胞,并首次提出(out)了(Got it)循環腫瘤細胞(CTC)的(of)概念1。1976年,Nowell将CTC的(of)定義修正爲(for):來(Come)源于(At)原發腫瘤或轉移腫瘤,獲得脫離基底膜的(of)能力并入侵通過組織基質進入血管的(of)腫瘤細胞。上(superior)世紀90年代,科學家開始對CTC的(of)臨床意義進行研究。2000後,CTC日益成爲(for)臨床上(superior)液态活檢标志物的(of)研究熱點,并在(exist)臨床越來(Come)越廣泛的(of)應用(use)3,4。
2. CTC的(of)特點3-5
2.1 可能是(yes)單個(indivual)細胞從病竈脫落進入外周血,也可能是(yes)成簇脫落;
2.2 不(No)同CTC在(exist)形态上(superior)有較大(big)差别;
2.3 CTC有很強的(of)異質性,不(No)同類型的(of)腫瘤CTC差别很大(big),即使同一(one)病人(people)來(Come)源的(of)不(No)同CTC細胞表所表達的(of)标志物種類及表達量也有差異;
2.4 CTC可能在(exist)循環過程中發生(born)上(superior)皮間質轉化(EMT)逐漸喪失上(superior)皮标志物;
2.5血液中存在(exist)可檢測CTC的(of)患者比例随癌症類型的(of)不(No)同而不(No)同。比如結直腸癌、卵巢癌和(and)乳腺癌大(big)約是(yes)50-70%,而非小細胞肺癌則低至30%;
2.6 CTC活力強,有抗脫巢凋亡活性;
2.7 CTC有侵襲和(and)轉移潛能。

圖1. CTC的(of)特點
(二)CTC檢測技術
血液中大(big)部分成分是(yes)白細胞和(and)紅細胞,CTC所占的(of)比例相對較少。每10mL血液中,含有1億個(indivual)白細胞和(and)500億個(indivual)左右紅細胞,而CTC的(of)數目可能僅有幾個(indivual)到(arrive)幾十個(indivual)。想要(want)準确地(land)檢測CTC細胞數目依賴非常靈敏的(of)檢測手段。近年來(Come)随着現代醫學研究技術的(of)進步和(and)CTC臨床應用(use)價值凸顯,許多研究機構和(and)研發團隊都在(exist)推出(out)不(No)同的(of)CTC檢測技術。CTC檢測技術包括CTC的(of)富集(分離)和(and)CTC的(of)分析鑒定(識别)等5。
1、CTC富集(分離)
1.1 免疫親和(and)法
建立在(exist)免疫親和(and)原理上(superior)的(of)CTC富集方法,利用(use)特異性抗體與細胞表面抗原進行特異性結合來(Come)富集CTC。基于(At)免疫親和(and)的(of)方法也分爲(for)很多種5:
1.1.1免疫磁珠法:以(by)CellSearch®法爲(for)代表,在(exist)磁珠上(superior)包被細胞表面粘附分子EpCAM,來(Come)捕獲CTC。臨床研究證明該方法檢測出(out)的(of)CTC數目與腫瘤的(of)預後密切相關。FDA已批準CellSearch®檢測的(of)CTC數目用(use)于(At)預測轉移性乳腺癌,前列腺癌,結直腸癌的(of)預後。
1.1.2微流體法:Nagrath和(and)Toner的(of)團隊研發了(Got it)一(one)種用(use)于(At)捕獲CTC的(of)微流體。上(superior)面有78,000個(indivual)微柱與EpCAM的(of)抗體相結合,可直接捕獲全血中的(of)CTC。整個(indivual)微流體共有970 mm2的(of)表面積,在(exist)2mL/hour的(of)通量下,CTC捕獲效率>60%,特異性在(exist)50%左右。在(exist)多種轉移腫瘤中該方法已被證明有較高的(of)CTC捕獲效率。
1.1.3納米結構基體:Wang et al等人(people)将EpCAM抗體結合在(exist)矽質的(of)納米基體上(superior),進行CTC捕獲。1mL/hour的(of)通量下,可以(by)達到(arrive)95%以(by)上(superior)的(of)捕獲效率。一(one)項研究利用(use)該方法對26例前列腺癌進行檢測,CTC的(of)檢出(out)率爲(for)20/26,明顯高于(At)CellSearch®系統(8/26)。
1.1.4微量離心管:由Hughes et al研制,在(exist)微量離心管上(superior)包被EpCAM及PSMA的(of)抗體,4.8mL/hour的(of)通量下,捕獲率可達50%,特異性達66%。用(use)該方法對14例轉移性腫瘤患者進行CTC檢測,檢出(out)率爲(for)100%,明顯高于(At)CellSearch®系統(9/14)。
1.1.5體内富集:将結合EpCAM的(of)裝置從前臂靜脈插入病人(people)體内,并停留30min,從而進行體内CTC富集。臨床實驗證明這(this)種方法對乳腺癌和(and)肺癌的(of)CTC細胞均有較高的(of)捕獲效率。
1.1.6白細胞去除法:屬于(At)陰性富集法。用(use)特異性抗體CD45,CD14等與白細胞結合,從而去除全血中的(of)白細胞。該方法比其它富集方法捕獲效率更高,但特異性明顯低于(At)其它方法。
利用(use)抗原抗體相互作(do)用(use)原理的(of)CTC富集方法可得到(arrive)較高的(of)純度。但捕獲效率對細胞表面抗原的(of)表達情況依賴較明顯。對于(At)依賴EpCAM的(of)捕獲方法,CTC捕獲效率與細胞表皮抗原的(of)表達情況密切相關,一(one)些CTC可能由于(At)EMT過程中表皮抗原發生(born)變化而未被捕獲。另外EpCAM法僅限于(At)對上(superior)皮來(Come)源的(of)CTC進行檢測。相對于(At)其它方法,免疫親和(and)法對CTC的(of)富集效率偏低。
1.2 物理特性富集法
依據CTC的(of)物理特性,如密度、大(big)小、可變形性及表面電荷等進行富集。